Назив производа:Метил етил кетон
Молекуларни формат:C4H8O
CAS број:78-93-3
Молекуларна структура производа:
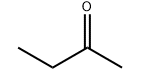
Спецификација:
| Ставка | Јединица | Вредност |
| Чистоћа | % | 99,8 мин |
| Боја | АФА | 8max |
| Киселинска вредност (као ацетатна киселина) | % | 0,002 макс. |
| влага | % | 0,03 макс. |
| Изглед | - | Безбојна течност |
Хемијска својства:
Метил етил кетон је подложан разним реакцијама због своје карбонилне групе и активног водоника поред карбонилне групе. Кондензација се дешава када се загрева хлороводоничном киселином или натријум хидроксидом да би се добио 3,4-диметил-3-хексен-2-он или 3-метил-3-хептен-5-он. Када се изложи сунчевој светлости дуже време, стварају се етан, сирћетна киселина и производи кондензације. Диацетил се ствара када се оксидује азотном киселином. Када се оксидује јаким оксидационим средствима као што је хромна киселина, ствара се сирћетна киселина. Бутанон је релативно стабилан на топлоту, а термичко разлагање на вишим температурама производи енон или метил енон. Када се кондензује са алифатичним или ароматичним алдехидима, стварају се кетони високе молекулске тежине, циклична једињења, кондензација кетона и смоле. На пример, кондензација са формалдехидом у присуству натријум хидроксида прво производи 2-метил-1-бутанол-3-он, након чега следи дехидрација до метакрилатона.
До резинизације долази након излагања сунчевој светлости или УВ светлости. Кондензација са фенолом даје 2,2-бис(4-хидроксифенил)бутан. Реагује са алифатичним естрима у присуству базног катализатора да би се произвели β-дикетони. Ацилација са киселим анхидридом у присуству киселог катализатора да би се формирали β-дикетони. Реагује са водоник цијанидом да би се формирао цијанохидрин. Реагује са амонијаком да би се формирали деривати кетопиперидина. α-атом водоника бутанона се лако супституише халогенима да би се формирали различити халогеновани кетони, као што је 3-хлоро-2-бутанон интеракцијом са хлором. Интеракција са 2,4-динитрофенилхидразином производи жути 2,4-динитрофенилхидразон.
Примена:
Метил етил кетон (2-бутанон, етил метил кетон, метил ацетон) је органски растварач релативно ниске токсичности, који се налази у многим применама. Користи се у индустријским и комерцијалним производима као растварач за лепкове, боје и средства за чишћење, као и као растварач за уклањање воска. Метил етил кетон, природна компонента неких намирница, може се испустити у животну средину вулканима и шумским пожарима. Користи се у производњи бездимног барута и безбојних синтетичких смола, као растварач и за површинске премазе. Такође се користи као ароматична супстанца у храни.
МЕК се користи као растварач за различите системе премаза, на пример, винил, лепкове, нитроцелулозу и акрилне премазе. Користи се у средствима за скидање боја, лаковима, спреј бојама, заптивачима, лепковима, магнетним тракама, штампарским бојама, смолама, колофонијумима, растворима за чишћење и за полимеризацију. Налази се у другим производима широке потрошње, на пример, цементима за домаћинство и хоби, и производима за пуњење дрвета. МЕК се користи у девоскинацији мазива, одмашћивању метала, у производњи синтетичке коже, провидног папира и алуминијумске фолије, и као хемијски међупроизвод и катализатор. То је растварач за екстракцију у преради прехрамбених производа и састојака хране. МЕК се такође може користити за стерилизацију хируршке и стоматолошке опреме.
Поред производње, извори МЕК-а у животној средини укључују издувне гасове из млазних и мотора са унутрашњим сагоревањем, као и индустријске активности попут гасификације угља. Налази се у значајним количинама у дуванском диму. МЕК се производи биолошки и идентификован је као производ микробног метаболизма. Такође је пронађен у биљкама, феромонима инсеката и животињским ткивима, а МЕК је вероватно мањи производ нормалног метаболизма сисара. Стабилан је под нормалним условима, али може да формира пероксиде при дужем складиштењу; они могу бити експлозивни.
Категорије производа
-

Телефон
-

Е-пошта
-

WhatsApp
-

Врх













